Золотые стандарты в лечении мигрени

- Главная
- >О клинике
- >Стандарты лечения
принципы доказательной медицины

В клинике головной боли и вегетативных расстройств им. Вейна мы проводим лечение заболеваний в соответствии со стандартами Минздрава РФ, учитывая международные стандарты. Врачи клиники в своей практике применяют подход доказательной медицины. Применение подхода доказательной медицины подразумевает такой подход, при котором решения о применении профилактических, диагностических и лечебных мероприятий принимаются исходя из имеющихся доказательств их эффективности и безопасности. Известно, что многие, даже существующие длительное время медицинские традиции и «общепризнанные» методы до сих пор не были подвергнуты адекватной научной проверке. Врачи нашей клиники в основном используют методы лечения, прошедшие научную проверку и соответствующие принципам доказательной медицины уровня IА.
Уровень доказательной медицины IА означает, что на данные методы были проведены большие двойные слепые плацебоконтролируемые исследования, а также использованы данные, полученные при мета-анализе нескольких рандомизированных контролируемых исследований.
Это означает, что в нашей клинике вы получаете только научно проверенное и доказанное лечение и самые современные методики.
Основные принципы доказательной медицины:
- В основе доказательной медицины лежит проверка эффективности и безопасности методик диагностики, профилактики и лечения. Под практикой доказательной медицины подразумевают использование данных, полученных из клинических исследований в повседневной клинической работе врача.
- В большинстве стран стали общепризнанными некоторые правила проведения клинических исследований.
- Результаты этих исследований позволяют пересмотреть устаревшие взгляды на определенную проблему с позиции доказательной медицины и отбросить малоэффективные и даже опасные методы лечения заболеваний.
Стандарты лечения головной боли напряжения Минздрава РФ
*выдержка из стандартов Минздрава РФ
Рекомендуется три подхода к лечению ГБН: поведенческая терапия, купирование болевых эпизодов и профилактическое лечение.
Препараты для профилактического лечения ГБН
- Амитриптилин – уровень рекомендации IA
- Митразапин – уровень рекомендации B
- Венлафаксин – уровень рекомендации B
- Кломипрамин – уровень рекомендации B и др. препараты уровня доказательной медицины класса B
Эффект антидепрессантов обусловлен их собственным противоболевым действием вследствие усиления активности антиноцицептивных (противоболевых) систем. Анальгетическое действие антидепрессантов наступает раньше, чем собственно антидепрессивное действие и в меньших дозах.
Немедикаментозное лечение
- Психо-поведенческие методы Электромиографическая биологическая обратная связь (ЭМГ-БОС)- уровень рекомендация АI
Рекомендуется комбинировать фармакологическое лечение ГБН с немедикаментозными методами.
Рекомендуется метод биологической обратной связи по электромиограмме перикраниальных мышц (ЭМГ-БОС) для обучения пациентов с ГБН психологическому и мышечному расслаблению. Экспериментальные работы указывают на активацию антиноцицептивных систем с увеличением уровня β-эндорфинов в плазме крови на фоне применения БОС. Серия повторных сеансов (от 8 до 15) позволяет существенно снизить частоту эпизодов головной боли напряжения и уровень тревоги. Рекомендуется когнитивно-поведенческая терапия (КПТ) и методы релаксации для уменьшения эмоционального напряжения.
Стандарты лечения мигрени Минздрава РФ
*выдержка из стандартов Минздрава РФ по лечению мигрени
Диагностика мигрени
Диагностика мигрени является исключительно клинической и основана на данных анамнеза, тщательном анализе характеристик головной боли и их соответствии диагностическим критериям МКГБ. Диагностическую ценность имеет дневник головной боли, который позволяет отличить приступ мигрени от приступа головной боли напряжения и других форм головной боли, а также выявить злоупотребление обезболивающими препаратами.
Лечение мигрени
Лечение мигрени в первую очередь направлено на облегчение течения заболевания (приступов головной боли и межприступного периода), улучшение качества жизни пациентов и предотвращение хронизации заболевания. Лечение мигрени включает: 1) купирование болевого приступа; 2) профилактическую терапию; 3) обучение пациента (поведенческую терапию). Лечение пациентов с неосложненной мигернью может осуществляться на этапе первичной помощи как неврологом, так и врачом общей практики. Пациенты с тяжелым течением мигрени, в т. ч. с хронической мигренью, множественными коморбидными нарушениями, лекарственным абузусом оптимально должны наблюдаться в специализированных центрах головной боли.
Лечение приступа мигрени направлено на уменьшение интенсивности, длительности болевого эпизода и сопутствующих симптомов, а также на восстановление общего состояния пациента. Для купирования приступа мигрени используются анальгетики и/или НПВС (предпочтительно некомбинированные), триптаны, реже эрготамин-содержащие препараты. Лечение приступа следует начинать как можно раньше (в течение первых 30 мин приступа). У пациентов с непродолжительным анамнезом мигрени и легкими приступами хороший эффект оказывают простые анальгетики.
Препараты для лечения мигрени
Анальгетики, обладающие доказанной эффективностью в купировании приступа мигрени:
- Ацетилсалициловая кислота – уровень рекомендаций IА
- Ибупрфен – уровень рекомендаций IА
- Напроксен – уровень рекомендаций IА
- Диклофенак – уровень рекомендаций IА
- Парацетамол – уровень рекомендаций IА
Наибольшей эффективностью и высоким уровнем доказательности (А) обладают специфические препараты – агонисты серотониновых рецепторов типа триптаны, показанием к применению которых является купирование приступа мигрени. Триптаны обладают преимуществом у пациентов с исходно тяжелыми приступами и выраженной дезадаптацией, а также при длительном анамнезе мигрени, когда эффективность анальгетиков существенно снижается.
- Суматриптан – уровень рекомендаций IА
- Элетриптан – уровень рекомендаций IА
- Золмитриптан – уровень рекомендаций IА
- Наратриптан – уровень рекомендаций IА
Лекарственные средства с доказанной эффективностью, рекомендуемые для профилактики мигрени
- B-блокаторы – уровень рекомендаций IА
- Антогонисты рецепторов ангиотензина – уровень рекомендаций IА
- Антикольвунсанты – уровень рекомендаций IА
- Ботулотоксин типа А – уровень рекомендаций IА
- Антидепрессанты – уровень рекомендаций В
Профилактическое лечение показано пациентам с частой эпизодической и хронической формами мигрени. Превентивное лечение направлено на снижение частоты и тяжести приступов, преодоление злоупотребления лекарственными препаратами для купирования головной боли, лечение коморбидных нарушений и повышение качества жизни пациентов.
-

Наприенко Маргарита Валентиновна
Главный врач, доктор медицинских наук, профессор, невролог высшей категории -

Филатова Елена Глебовна
Невролог, профессор, доктор медицинских наук -

Екушева Евгения Викторовна
Невролог, доктор медицинских наук, профессор -

Латышева Нина Владимировна
Невролог, кандидат медицинских наук
Источник
Мигрень – частая форма первичной головной боли, которая значительно ухудшает качество жизни молодых трудоспособных пациентов. Распространенность мигрени в странах Европы и США в среднем составляет 14%, значительно чаще мигрень встречается у женщин [1]. Для мигрени характерна интенсивная, приступообразная, чаще односторонняя головная боль длительностью от 4 до 72 ч, усиливающаяся при физической активности и сопровождающаяся различными неврологическими, соматическими, эмоционально-аффективными и вегетативными проявлениями. Существуют 2 формы мигрени: мигрень без ауры и мигрень с аурой [2].
У большинства пациентов мигрень имеет наследственный характер, но среди основных механизмов также обсуждаются нейрохимические и нейрогенные факторы. Показано также, что для пациентов с мигренью характерна повышенная возбудимость нейронов коры головного мозга. Важным механизмом, запускающим приступ и обусловливающим развитие и сохранение боли, является активация тригемино-васкулярной системы (ТВС). Механизм мигренозной ауры связывают с распространением волны возбуждения корковых нейронов (распространяющаяся корковая депрессия) от зрительной коры к соматосенсорной и лобно-височной области. Распространяющаяся корковая депрессия определяет характер и последовательность симптомов ауры: зрительных, чувствительных, речевых [3].
Большинство приступов мигрени возникают внезапно. Но часто приступ может провоцироваться рядом эндогенных и экзогенных факторов (триггеров мигрени). Многие авторы полагают, что для запуска приступа мигрени необходимо сочетание нескольких триггеров. В настоящее время описано около 60 различных факторов, провоцирующих приступы мигрени [4].
Основные факторы, провоцирующие приступ мигрени:
– психофизиологические: чрезмерная нагрузка, усталость, плохой или избыточный сон;
– гормональные и соматические: менструация, применение оральных контрацептивов, высокое кровяное давление;
– эмоциональные: тревога, депрессия, выраженный стресс;
– диетические: нерегулярное питание, алкоголь, шоколад, сыр, цитрусовые и др.;
– экзогенные: изменение погоды и климата, яркий свет, шум, сильные запахи, курение, горячая ванна.
Диагностика мигрени – клиническая, т. е. она основывается на детальном клиническом опросе и осмотре пациента. Крайне важны информация о возрасте начала головной боли, семейный анамнез, характеристики приступа, провоцирующие и облегчающие факторы, отсутствие признаков вторичного характера головной боли. При установлении диагноза следует опираться на диагностические критерии Международной классификации головных болей МКГБ-3 бета [2].
При типичной клинической картине мигрени дополнительные исследования не показаны, поскольку они неинформативны. Параклинические исследования должны проводиться только при подозрении относительно симптоматического характера цефалгии.
Основные стратегии купирования приступа мигрени
Главные цели лечения мигрени – облегчение течения мигрени, предотвращение хронизации и улучшение качества жизни пациента. Для достижения вышеперечисленных целей необходимо соблюдение нескольких подходов [5]:
1) купирование приступов мигрени;
2) профилактическое лечение;
3) рекомендации по соблюдению стиля жизни и поведенческая терапия.
Профилактическая терапия мигрени проводится пациентам в случае наличия соответствующих показаний (частые приступы головной боли, высокая степень дезадаптации пациента, полная неэффективность симптоматических средств и др.). В целом от 10 до 30% пациентов нуждаются в назначении превентивных средств для снижения частоты приступов. Между тем стратегия купирования приступов должна быть применима у каждого пациента, обратившегося за консультацией, поскольку тяжесть мигренозной цефалгии, как правило, требует лекарственного купирования, причем подавляющее большинство пациентов лекарственные средства используют при каждом приступе мигрени.
Цели купирования приступа мигрени – уменьшение интенсивности, длительности боли и сопровождающих симптомов (тошнота, рвота, фоно- и фотофобии и т. д.) и нормализация общего состояния пациента. Выбор оптимального средства для купирования приступа мигрени среди существующего множества фармакологических средств является непростым для каждого пациента.
Фармакологические средства, применяемые для купирования приступа мигрени:
• Препараты с неспецифическим механизмом действия:
– анальгетики (парацетамол, кодеин);
– нестероидные противовоспалительные средства;
– комбинированные препараты.
• Специфические антимигренозные средства:
– селективные агонисты 5-HT1В/1D-рецепторов (триптаны);
– неселективные агонисты 5-HT1-рецепторов (эрготамин, дигидроэрготамин).
При выборе конкретного препарата для купирования приступа следует учитывать индивидуальные характеристики пациента, такие как интенсивность головной боли, скорость ее нарастания, наличие ассоциированных симптомов, степень дезадаптации, предшествующий опыт и предпочтения пациента. С этой точки зрения используется стратифицированный подход, который предполагает учет наиболее важной характеристики приступа мигрени – уровня дезадаптации пациента. Этот подход основывается на ранжировании мигренозных приступов по тяжести и степени нарушения адаптации пациентов [6]. Пациентам с легкими приступами и хорошим уровнем адаптации назначаются простые анальгетики и НПВС, возможно, в комбинации с лекарствами, которые улучшают их абсорбцию. Пациентам с тяжелыми и умеренными приступами необходимо назначение триптанов.
Также важным принципом купирования приступа мигрени является раннее назначение антимигренозного препарата, обеспечивающее более полный обезболивающий эффект и меньшую вероятность рецидива. Кроме того, по мере прогрессирования приступа у большинства пациентов развивается гастропарез с нарушением пассажа пер-оральных медикаментозных препаратов в кишечник и их плохой абсорбцией. Раннее применение антимигренозных средств важно и с этой точки зрения [7].
Триптаны создавались специально для лечения приступа мигрени. Они обладают высоким аффинитетом к 5-HT1D и 5-HT1В-рецепторам, и у них отсутствует активность по отношению к адренергическим, дофаминергическим, мускариновым, гистаминовым и серотониновым рецепторам других подтипов.
В настоящее время известны 7 представителей класса триптанов, в России зарегистрированы 5 из них (табл. 1) [8]. 
Патофизиологические механизмы действия триптанов при мигрени:
– сужение избыточно расширенных краниальных сосудов;
– ингибирование выделения противовоспалительных и вазоактивных пептидов;
– ингибирование трансмиссии боли на уровне ствола мозга.
Несмотря на то, что все препараты относятся к одному классу, они имеют различные фармакокинетические параметры. Эти различия имеют большое клиническое значение как факторы, определяющие эффективность триптана.
В 1990 г. в клиническую практику был внедрен суматриптан. Он был первым представителем класса триптанов. В клинических исследованиях и до настоящего времени суматриптан рассматривается как «золотой стандарт» специфического лечения приступов мигрени. В последующем в практику вошли препараты с более высокой биодоступностью, достаточно длинным периодом полувыведения, что позволяет избегать частого приема препарата и рецидива головной боли.
Сравнительный анализ триптанов для купирования приступа мигрени
В исследовании J. Pascual et al. был проведен анализ использования золмитриптана в дозировке 5 мг для купирования приступа мигрени. Были исследованы 82 пациента, которые купировали в среднем 7 приступов мигрени. Пациенты принимали золмитриптан орально и интраназально, и также суматриптан подкожно. Авторами был сделан вывод о том, что около 62,5% пациентов отдавали свое предпочтение золмитриптану в связи с его хорошей эффективностью [9].
В 2015 г. было проведено подобное исследование, авторы которого пришли к выводу о том, что стандартная доза триптанов уменьшала интенсивность головной боли в течение 2 ч у 42–76% пациентов. Среди триптанов лучшую эффективность показали подкожная форма суматриптана и таблетированные формы золмитриптана и элетриптана [10].
Эффективность золмитриптана для купирования острого приступа мигрени была показана в исследовании L.C. Chen et al. Авторы продемонстрировали, что золмитриптан в дозировке 2,5 мг имел такую же эффективность при острых приступах мигрени, как элетриптан 2,5 мг и суматриптан 50 мг. Также золмитриптан был более эффективен, чем наратриптан 2,5 мг [11].
Золмитриптан является селективным агонистом 5НТ1-рецепторов. Обладает высоким сродством по отношению к 5НТ1B/1D-рецепторам и умеренным аффинитетом к 5HT1A-рецепторам. Взаимодействуя с 5НТ-рецепторами интракраниальных сосудов (включая артериовенозные анастомозы) и чувствительных нервов ТВС, иннервирующих чувствительные к боли интракраниальные структуры, золмитриптан вызывает вазоконстрикцию, ассоциированную с подавлением высвобождения CGRP, VIP и субстанции Р, и облегчает течение приступа мигрени, снижая интенсивность боли не позднее чем через 1 ч после приема, уменьшая выраженность тошноты, рвоты, фото- и фонофобии. Взаимодействие золмитриптана с рецепторами по механизму отрицательной обратной связи способствует уменьшению высвобождения серотонина и снижению его содержания в синаптической щели. Кроме этого, золми-триптан оказывает действие на центры ствола головного мозга, ответственные за развитие мигрени, что объясняет устойчивый повторный эффект при лечении серии приступов мигрени у одного пациента.
После приема внутрь золмитриптан быстро и хорошо всасывается в пищеварительном тракте; прием пищи не влияет на абсорбцию препарата. Абсолютная биодоступность — около 40%. Максимальная концентрация в плазме крови достигается через 2 ч после приема. Средний период полувыведения золмитриптана и его активного метаболита — около 3 ч. Связывание с белками плазмы крови низкое (приблизительно 25%). Метаболизируется препарат в печени с образованием активного N-десметил-метаболита и двух неактивных — индолуксусной кислоты и N-оксид-метаболита. Агонистическое влияние активного метаболита в отношении 5НТ1-рецепторов в 2–6 раз превосходит исходное соединение. При повторном приеме аккумуляция не наблюдается. Более 60% введенной дозы выводится с мочой преимущественно в виде индолуксусного метаболита и около 30% — с калом в неизмененном виде. Почечный клиренс золмитриптана и его метаболитов у пациентов с умеренной и выраженной почечной недостаточностью уменьшен в 7–8 раз. Известно, что фармакокинетика золмитриптана не изменяется у лиц пожилого возраста [12].
В исследовании С.М. Spencer et al. была показана эффективность золмитриптана при лечении мигрени, связанной с менструацией, и мигрени с аурой, персистирующей и/или повторяющейся мигрени. Также золмитриптан был эффективен при облегчении таких симптомов мигрени, как тошнота, фото- и фонофобия. Для облегчения головной боли при мигрени золмитриптан в дозировке 5 мг имел сходную эффективность с суматриптаном в дозе 100 мг при однократном приступе, но, как правило, был более эффективен, чем суматриптан в дозах 25 и 50 мг для многократных приступов. Золмитриптан, как правило, хорошо переносится пациентами, вызывает меньшее количество нежелательных побочных эффектов. Наиболее частыми нежелательными явлениями при терапии золмитриптаном являются астения, сухость во рту, тошнота, головокружение, сонливость, парестезия, боль в груди [13].
В крупном двойном рандомизированном исследовании сравнивали эффективность и переносимость золмитриптана (2,5 или 5 мг) и суматриптана (50 мг) для купирования до 6 умеренных и тяжелых приступов мигрени. В исследовании приняли участие 1522 пациента, из них 500 пациентов принимали золмитриптан 2,5 мг, 514 пациентов – золмитриптан в дозировке 5 мг, 508 пациентов – 50 мг суматриптана. В целом уменьшение интенсивности головной боли в течение 2 ч в этих группах составило 62,9%, 65,7% и 66,6% соответственно. Не было статистически значимых различий между 50 мг суматриптана и 2,5 мг золмитриптана (р = 0,12) или 5 мг (р = 0,80). Авторы пришли к выводу, что золмитриптан (2,5 или 5 мг) оказался столь же эффективным, как и суматриптан в дозировке 50 мг [14]. Однако в сравнительном исследовании была показана более высокая эффективность купирования приступа мигрени в течение 2 ч золмитриптаном в дозировке 2,5 мг, чем суматриптаном в дозировке 25 и 50 мг, хотя у 3,3% пациентов не было клинически значимых показателей. В данном исследовании авторами не было обнаружено различий в частоте побочных эффектов между золмитриптаном и суматриптаном [15].
В большом сравнительном исследовании 1445 пациентов с мигренью оценивалась эффективность золмитриптана (в дозе 2,5 мг и 5 мг) и суматриптана (в дозе 25 мг и 50 мг) [16]. Поскольку для большинства современных триптанов характерно купирование 2-х атак из 3-х, в данном исследовании анализировалось количество пациентов с постоянным эффектом (в 3-х последовательных приступах). Этот показатель был достоверно выше в группе золмитриптана (рис. 1).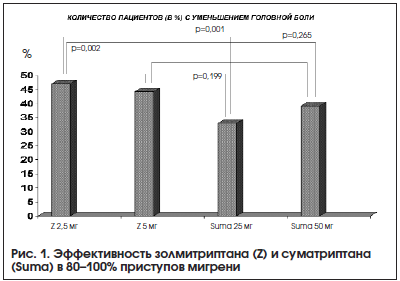
Триптаны противопоказаны при ишемической болезни сердца (ИБС), инсульте в анамнезе, неконтролируемой артериальной гипертензии (АГ), приеме некоторых лекарственных средств [17].
Вопрос о кардиобезопасности применения триптанов изучался специально в масштабных клинических исследованиях. В период с 1995 по 1999 г. в 20 штатах США с целью выявления серьезных кардиоваскулярных последствий мигрени и установления их возможной связи с применением современных антимигренозных средств проведено одно из самых больших проспективных популяционных исследований. В нем приняли участие 130 тыс. больных мигренью и примерно такое же количество больных, не страдающих мигренозными головными болями. В этих группах в течение всего периода наблюдения изучалась частота значимых кардиоваскулярных событий: инфаркта миокарда, инсульта, сердечных аритмий, нестабильной стенокардии, транзиторных ишемических атак (ТИА). Также анализировалась частота указанных событий у принимавших (50 383 пациента) и не принимавших (80 028 пациентов) селективные агонисты 5-НТ рецепторов. В целом у больных мигренью была выявлена более высокая частота ИБС, цереброваскулярных заболеваний, АГ и гиперлипидемии, а также нестабильной стенокардии и ТИА по сравнению с лицами, не страдающими мигренозными цефалгиями. Было показано, что в группе больных мигренью среди использовавших и не использовавших триптаны не было достоверных различий по частоте инфарктов миокарда, инсультов, сердечных аритмий, нестабильной стенокардии и ТИА, а частота смертельных случаев у пациентов, использующих триптаны, была даже ниже. Эти результаты позволили авторам прийти к заключению, что использование триптанов у больных мигренью не сопровождается увеличением риска значимых сердечно-сосудистых событий [18].
Таким образом, изучение этих селективных свойств триптанов имеет большое практическое значение для обоснования кардиобезопасности современных представителей данной группы препаратов. Сопоставление результатов клинических и экспериментальных исследований не позволяет связывать появление так называемых триптан-ассоциированных кардиальных жалоб с объективными кардиоваскулярными нарушениями у пациентов с мигренью. Для их объяснения следует изучить другие возможные неишемические причины этих расстройств. Их наличие может быть обусловлено генерализованными вазоспастическими реакциями, нарушением моторики пищевода, легочного кровообращения либо энергетического метаболизма скелетных мышц грудной стенки, а также развитием процессов центральной сенситизации [2]. Случаи серьезных кардиоваскулярных событий как в клинических испытаниях, так и в клинической практике наблюдаются крайне редко, и их появление не связано с фактом применения пациентами триптанов для купирования приступов головной боли. Профиль безопасности триптанов хорошо изучен. В соответствии с данными клинических исследований для пациентов без признаков коронарного заболевания триптаны характеризуются низким риском серьезных кардиоваскулярных побочных эффектов. Это позволяет рекомендовать пациентам с низким риском коронарного заболевания триптаны без предварительной оценки кардиального статуса.
Таким образом, для купирования приступа мигрени могут использоваться различные препараты. Выбор оптимального средства для купирования приступа мигрени среди существующего множества фармакологических средств является непростым для каждого пациента. С этой точки зрения оптимален стратифицированный подход, основанный на ранжировании мигренозных приступов по тяжести и степени нарушения адаптации пациентов. Пациентам с тяжелыми и умеренными приступами необходимо назначение специфических препаратов (триптанов) с учетом их высокой эффективности в клинических исследованиях. Так, основываясь на данных эффективности золми-триптана в сравнительных исследованиях, можно рекомендовать данный препарат в качестве приоритетного для симптоматической терапии мигрени. Также для успешного лечения необходимо динамическое наблюдение за пациентами. Крайне важно помнить, что допустимо для купирования приступов использовать не более 10 доз в месяц, чтобы избежать злоупотребления лекарствами и развития медикаментозно-индуцированной головной боли.
Источник
