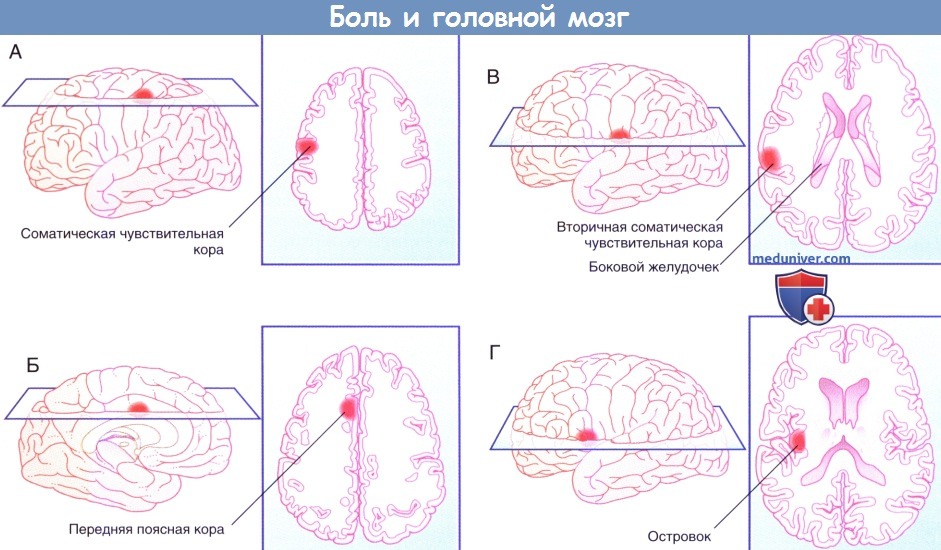
Роль структур головного мозга в формировании боли
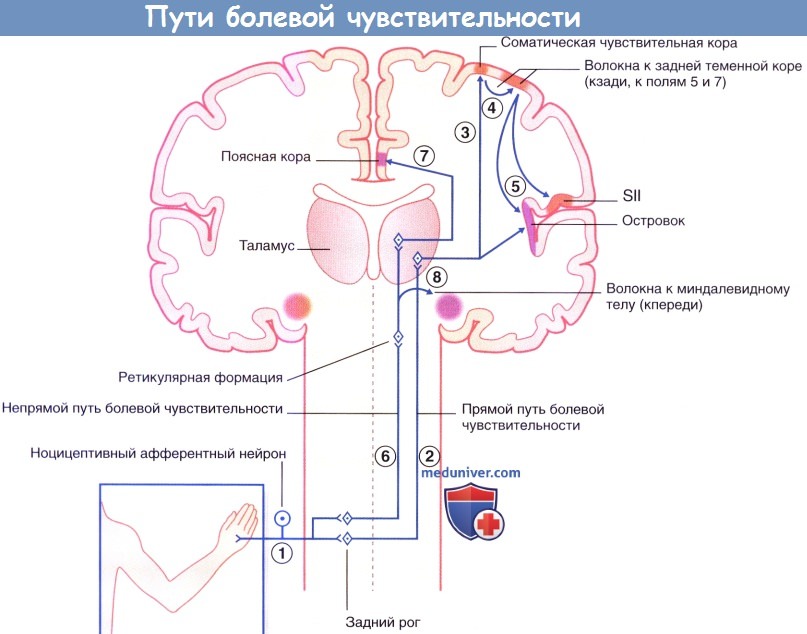
Полноценное чувственное восприятие боли организмом без участия коры головного мозга невозможно. Ретикулярная формация ствола (РФ) передает болевую информацию в неспецефические ядра таламуса, затем в кору, а также в гипоталамус и лимбическую систему, усиливает и пролонгирует защитные реакции спинного мозга и ствола, вовлекает в ответ вегетативную (особенно симпатическую) нервную систему. Повышение активирующего влияния восходящей РФ вызывает реакции возбуждения, настораживания.
Первичное проекционное поле болевого анализатора находится в соматосенсорной коре задней центральной извилины. Оно обеспечивает восприятие «быстрой» боли и идентификацию места ее возникновения на теле. Для более точной идентификации локализации боли в процесс обязательно включается и нейроны моторной коры передней центральной извилины.
Вторичное проекционное поле расположено в соматосенсорной коре на границе пересечения центральной борозды с верхним краем височной доли. Нейроны данного поля имеют двусторонние связи с ядрами таламуса, что позволяет этому полю избирательно фильтровать, проходящие через таламус возбуждения болевого характера. А это в свою очередь позволяет данному полю вовлекаться в процессы, связанные с извлечением из памяти энграммы необходимого поведенческого акта, его реализации в деятельности эффекторов и оценки качества достигнутого полезного результата. Двигательные компоненты болевого поведения формируются в совместной деятельности моторной и премоторной коры, базальных ганглиев и мозжечка.
Таламус учавствует в передаче и переработке болевой информации: специфические ядра таламуса обеспечивают анализации болевого раздражения, его силы и длительности, неспецифические ядра таламуса учавствуют в формировании мотивационно-аффективного аспекта боли.
Лобная кора играет важную роль в восприятии боли. Она обеспечивает самооценку боли (ее когнитивный компонент) и формирование целенаправленного болевого поведения.
Лимбическая система (поясная извилина, гиппокамп, зубчатая извилина, миндалевидный комплекс височной доли) получает болевую информацию от передних ядер таламуса и формирует эмоциональный компонент боли, запускает вегетативные, соматические и поведенческие реакции, обеспечивающие приспособительные реакции к болевому раздражителю.
Боль можно классифицировать следующим образом:
1. Ноцигеная.
2. Нейрогенная.
3. Психогенная.
Ноцигеная боль. Когда при раздражении кожных ноцицепторов, ноцицепторов глубоких тканей или внутренних органов тела, возникающие импульсы, следуя по классическим анатомическим путям, достигают высших отделов нервной системы и отображаются сознанием, формируется ощущение боли. Боль от внутренних органов возникает вследствие быстрого сокращения, спазма или растяжения гладких мышц, поскольку сами гладкие мышцы нечувствительны к жару, холоду или рассечению. Боль от внутренних органов, особенно имеющих симпатическую иннервацию, может ощущаться в определённых зонах на поверхности тела. Такая боль называется отражённой. Наиболее известные примеры отражённой боли – боль в правом плече и правой стороне шеи при поражении желчного пузыря, боль в нижней части спины при заболевании мочевого пузыря и, наконец, боль в левой руке и левой половине грудной клетки при заболеваниях сердца. Нейроанатомическая основа этого феномена не совсем понятна. Возможное объяснение состоит в том, что сегментарная иннервация внутренних органов та же, что и отдалённых областей поверхности тела.
Нейрогенная боль. Этот тип боли может быть, определён, как боль вследствие повреждения периферической или центральной нервной системы и не объясняется раздражением ноцицепторов. Такая боль имеет ряд особенностей, отличающих её, как клинически, так и патофизиологически от ноцигенной боли:
1. Нейрогенная боль имеет характер дизестезии. Хотя дескрипторы: тупая, пульсирующая или давящая являются наиболее частыми для подобной боли, патогномоничными характеристиками для неё считаются определения: обжигающая и стреляющая.
2. В огромном большинстве случаев нейрогенной боли отмечается частичная потеря чувствительности.
3. Характерны вегетативные расстройства, такие как снижение кровотока, гипер и гипогидроз в болевой области. Боль часто усиливает или сама вызывает эмоционально-стрессовые нарушения.
4. Обычно отмечается аллодиния (означающая болевое ощущение в ответ на низко интенсивные, в нормальных условиях не вызывающие боли раздражители). Например, лёгкое прикосновение, дуновение воздуха или причёсывание при тригеминальной невралгии вызывает в ответ “болевой залп”. Более ста лет назад Trousseau (1877) отметил сходство между пароксизмальной стреляющей болью при тригеминальной невралгии и эпилептическими припадками. В настоящее время известно, что все стреляющие нейрогенные боли могут лечиться антиконвульсантами.
Нейрогенная боль имеет много клинических форм. К ним можно отнести некоторые поражения периферической нервной системы, такие как постгерпетическая невралгия, диабетическая невропатия, неполное повреждение периферического нерва, особенно срединного и локтевого (рефлекторная симпатическая дистрофия), отрыв ветвей плечевого сплетения. Нейрогенная боль вследствие поражения центральной нервной системы обычно бывает обусловлена цереброваскулярной катастрофой. Это то, что известно под классическим названием “таламического синдрома”, хотя недавние исследования показывают, что в большинстве случаев очаги поражения расположены в иных областях, чем таламус.
Многие боли клинически проявляются смешанными – ноцигенными и нейрогенными элементами. Например, опухоли вызывают повреждение тканей и компрессию нервов; при диабете ноцигенная боль возникает вследствие поражения периферических сосудов, нейрогенная – вследствие нейропатии; при грыжах межпозвонкового диска, компримирующих нервный корешок, болевой синдром включает жгучий и стреляющий нейрогенный элемент.
Психогенная боль. Утверждение что боль может быть исключительно психогенного происхождения, является дискуссионным. Широко известно, что личность пациента формирует болевое ощущение. Оно усилено у истерических личностей, и более точно отражает реальность у пациентов неистероидного типа.
Люди различных этнических групп отличаются по восприятию послеоперационной боли. Пациенты европейского происхождения отмечают менее интенсивную боль, чем американские негры или латиноамериканцы. У них также отмечается низкая интенсивность боли по сравнению с азиатами, хотя эти отличия не очень значительны.
Любое хроническое заболевание или недомогание, сопровождающееся болью, влияет на эмоции и поведение личности. Боль часто ведёт к появлению тревожности и напряжённости, которые сами увеличивают восприятие боли. Это поясняет важность психотерапии в контроле над болью. Биологическая обратная связь, релаксационный тренинг, поведенческая терапия и гипноз применяются в качестве психологического вмешательства и могут оказаться полезными в некоторых упорных, рефрактерных к лечению случаях. Лечение может быть более эффективным, если учитывает психологическую и другие системы (окружающую среду, психофизиологию, познавательную, поведенческую), которые потенциально влияют на болевое восприятие. Обсуждение психологического фактора хронической боли ведётся на основе теории психоанализа, с бихевиористских, когнитивных и психофизиологических позиций.
Поскольку эта тенденция имеет вышеупомянутые этнические и культуральные особенности, она кажется врождённой. Поэтому так заманчивы перспективы исследований, проводимых в настоящее время и направленных на поиск локализации и выделение “гена боли”.
Источник
Механизмы восприятия боли: головной мозг и больСогласно определению Международной ассоциации по изучению боли, боль — это неприятное чувствительное и эмоциональное переживание, связанное с истинным или потенциальным повреждением ткани или описываемое в терминах такого повреждения. В этом определении сделан акцент на аффективном (эмоциональном) компоненте боли. Другой компонент боли — чувствительно-дискриминационый («Где и как сильно?»). а) Периферические пути болевой чувствительности. За проведение болевых ощущений отвечают тонкие миелинизированные (А6) и немиелинизированные (С) волокна, исходящие от униполярных клеток спинномозгового ганглия. Иногда эти волокна называют «волокнами боли», хотя существуют и другие нервные волокна сравнимого диаметра, которые являются исключительно механорецепторными. В то же время другие волокна, связанные, например, с механорецепторами или терморецепторами, вызывают чувство боли только при работе на высокой частоте. В общем плане обсуждения боли последние волокна называют полимодальными ноцицепторами. В составе спинномозговых нервов находятся дистальные отростки ганглионарных клеток, иннервирующих соматические ткани, в том числе кожу, париетальную плевру и брюшину, мышцы, суставные капсулы и кости. Проксимальные отростки отдают ветви на уровне зоны выхода задних корешков, далее в составе дорсолатерального пути Лиссауэра поднимаются вверх, пропуская пять или более сегментов спинного мозга, а затем оканчиваются в пластинах I, II и IV заднего рога. Аналогичные волокна тройничного нерва оканчиваются в спинномозговом ядре тройничного нерва. Дистальные нервные отростки, направляющиеся от внутренних органов, имеют общую периневральную оболочку с постганглионарными волокнами симпатического ствола. Проксимальные отростки пересекаются с волокнами пути Лиссауэра и заканчиваются в этой же области. Считают, что перекрест соматических и висцеральных афферентных окончаний на дендритах центральных болевых нейронов объясняет возникновение отраженной боли при таких состояниях, как инфаркт миокарда или острый аппендицит.
б) Сенситизация ноцицепторов. При повреждении тканей из них происходит выброс различных активных веществ — брадикининов, простагландинов и лейкотриенов, которые понижают порог возбудимости ноцицепторов. При повреждении С-волокон происходит также активация аксон-рефлексов, в окружающие ткани высвобождаются субстанция Р и кальцитонин ген-связанный пептид (CGRP), стимулируя выброс гистамина тучными клетками. Гистаминовые рецепторы, которые могут располагаться на нервных окончаниях (Глава 8), способы стимулировать синтез арахидоновой кислоты за счет гидролиза мембранных фосфолипидов. Фермент циклооксигеназа превращает арахидоновую кислоту в простагландины. (Механизм действия аспирина и других нестероидных противовоспалительных препаратов заключается в угнетении этого фермента и снижении синтеза простагландинов.) В результате возникают длительная активация большого числа С-волокон и сенситизация механических ноцицепторов. Клинически это проявляется аллодинией, при которой даже легкое прикосновение к какой-то области вызывает болевые ощущения, и гипералгезией, когда даже незначительные болезненные стимулы воспринимают как сильнейшую боль. Для синдрома раздраженного кишечника характерна сенситизация ноцицептивных интерорецепторов брюшной стенки. Такой механизм развития болевого синдрома характерен также для интерстициального цистита. Сенситизация нейронов С-волокон может также происходить за счет изменения транскрипции генов, когда аномальные натриевые каналы встраиваются в клеточную мембрану нейронов заднего спинномозгового ганглия. В этом месте может возникать спонтанная электрическая активность, которая, как считают, может быть ответственна за неэффективность анальгетиков, блокирующих проведение нервного импульса на высоких уровнях. в) Нейропатическая боль. При рассечении периферического нерва его проксимальная и дистальная культи оказываются разделенными формирующейся рубцовой тканью. На аксонах, захваченных в этой рубцовой ткани, формируются небольшие нитевидные утолщения — невромы, которые очень чувствительны к сдавлению. При их длительной активации страдания пациента усиливаются, поскольку у него развивается синдром центральной боли. Постгерпетическая невралгия — это нейропатическая боль, которая становится следствием перенесенной инфекции herpes zoster («опоясывающий лишай») и проявляется появлением везикул вдоль зоны иннервации кожного нерва, обычно межреберного. Вирус может поддерживать боль за счет активации механизма транскрипции генов, который был описан выше. Центральные пути болевой чувствительности Центральные ноцицептивные нейроны подразделяют на две группы—специфические, с небольшой зоной периферической иннервации (около 1 см2), а также имеющие широкий динамический диапазон (более 2 см2). Это механические ноцицепторы, которые кодируют тактильные стимулы как импульсы низкой чистоты и болевые стимулы как импульсы высокой частоты. Согласно общепринятому мнению, спиноталамический путь (или переднебоковой, учитывая его расположение в спинном мозге) состоит из различных волокон, которые отвечают как за различение болевых, температурных и тактильных стимулов (неоспиноталамический, или прямой, путь), так и за аффективную, двигательную и вегетативную реакции на боль (палеоспиноталамический, или непрямой, путь).
г) Прямой путь болевой чувствительности. Прямой путь для туловища и конечностей начинается от заднего рога спинного мозга и в составе спиноталамического пути направляется к задней части вентрального заднелатерального ядра таламуса с противоположной стороны. На голове и шее он начинается в спинномозговом ядре тройничного нерва и по тройнично-таламическим волокнам идет к задней части медиального ядра противоположного таламуса. Отсюда волокна преимущественно направляются к первичной соматической чувствительной коре (SI) и частично к верхней части латеральной борозды (SII). Установлена соматотопическая организация этой области, что удалось выявить при помощи проведения ПЭТ головного мозга во время воздействия теплового стимула на различные участки лица. Благодаря исследованиям на животных обнаружили, что в SI имеются высоковозбудимые специфические ноцицептивные нейроны, рецепторное периферическое поле которых относительно невелико. Именно эти нейроны лучше всего отвечают на вопрос «Где и как сильно болит?». На рисунках ниже изображены проекции к задней теменной коре и SII. Понятно, что спиноталамическая система раннего оповещения отвечает за поворот глаз и головы в сторону источника боли. Спинопокрышечный путь направляется наверх вдоль спиноталамического пути и заканчивается в верхних холмиках. Он также организован соматотопически. Волокна этого пути обеспечивают работу зрительного рефлекса, который поворачивает глаза/туловище/конечности в сторону стимулируемой области. Помимо активации этого филогенетически древнего пути (он имеется уже у рептилий), зрительный путь, отвечающий на вопрос «Где?», также связан с волокнами, идущими к задней теменной коре от SI. В SII число ноцицептивных нейронов меньше, однако они также могут получать зрительную информацию. Они связаны с островком, который получает импульсы непосредственно от таламуса. При стимуляции островка в организме возникают вегетативные реакции (повышение частоты сердечных сокращений, вазоконстрикция, потоотделение). Интересно, что при повреждении островка человек перестает воспринимать болевые стимулы как неприятные, но при этом он все еще может локализовать стимул и определять его интенсивность. Такое состояние называют асимболией боли. д) Непрямой путь болевой чувствительности. Непрямой путь — полисинаптический, в составе спиноретикулярного и тройнично-ретикулярного путей он направляется к дорсальному медиальному ядру таламуса, проецируясь (в том числе) к передней поясной коре. Эта область отвечает за аффективный компонент боли. Доказательством этого служит тот факт, что у пациентов с хроническим болевым синдромом успешно выполняют хирургическое пересечение (цингулотомию) или удаление (цингулэктомию) поясной коры. Пациенты сообщают, что сила болевых ощущений не изменилась, но боль при этом не кажется им такой нестерпимой. Точно такой же эффект дают инъекции морфия, вероятно, потому, что в передней поясной коре сосредоточено наибольшее число опиоидных рецепторов. После цингулэктомии часто возникает отек участка мозга, осуществляющий контроль за мочевым пузырем. В связи с этим в течение какого-то времени пациентов может беспокоить недержание мочи. Однако, что важнее, более чем у половины больных после операции развивается «аффективное уплощение» — люди перестают испытывать как положительные, так и отрицательные эмоции. Резкий удар или внезапно возникшая боль любого происхождения способна вызвать у человека чувство страха. Его появление связано с активацией спиномезенцефалических волокон, идущих к ретикулярной формации среднего мозга, а также к миндалевидному телу и ядру мозга, которое в первую очередь отвечает за чувство страха (см. основной текст). Считают, что часть волокон может идти наверх в составе дорсолатерального пути Лиссауэра или рядом с ним; наличие этих волокон может объяснить сохранение болевого синдрома у некоторых из пациентов, перенесших хордотомию.
е) Центральная боль. Центральная боль практически всегда возникает вследствие активации центральных проецирующих боль нейронов (ЦПБН) спиноталамического и спиноретикулярного путей. За эти процессы отвечают следующие три механизма. • Длительная активация глутаматных NMDA-рецепторов стимулами от заднего корешка, которую наблюдают в течение нескольких недель или месяцев. В результате развивается долгосрочная потенциация ЦПБН. • Порог возбудимости ЦПБН может еще больше снижаться путем запуска транскрипции определенных генов за счет появления дополнительных глутаматных рецепторов на их нейронах. • Для третьего механизма лучше всего подходит определение «парадоксальный». Этот механизм уже описан в отдельной статье на сайте при обсуждении супраспинальной антиноцицептиеной системы, когда серотонинергические нейроны, проецирующиеся от большого ядра шва (БЯШ) среднего мозга, могут тормозить активность ЦПБН за счет активации энкефалинергических вставочных нейронов. Исследования на животных показали, что хотя для появления центральной боли может быть достаточно одного из первых двух механизмов, для ее поддержания необходимо, чтобы несеротонинергические нейроны БЯШ облегчили возбудимость ЦПБН. Действие этих нейронов обусловлено неизвестным возбуждающим нейромедиатором. Самый очевидный пример такой боли—фантомная боль, при которой сильные болевые ощущения возникают в дистальной части ампутированной конечности. Один из видов центральной боли — таламическая боль, которая возникает при инсульте в области белого вещества около заднего вентрального ядра таламуса. Появление сильнейшей боли в противоположной половине тела может быть связано с нарушением нормальных тормозных влияний, которые поступают в задние отделы таламуса от близлежащих ретикулярных ядер. – Также рекомендуем “Миндалевидное тело головного мозга: функции, проводящие пути” Редактор: Искандер Милевски. Дата публикации: 25.11.2018 |
Источник